R6年度 第1回基礎学力テスト、理科の問題分析(4)

本日は、最後となる「化学」の
理科の問題分析となります。
出題単元は、「溶解度」と
「酸化還元反応」でした。
どちらの問題も、原理を問う
すこし捻った問題であったと思います。
難易度的には「やや難」レベルです。
実際は、小学生レベルの計算問題なのですが
中3生で小学算数の概念理解をできている
生徒は多くはありませんからこの評価です。
今日は、そんなお話です。
大問5【中1化学】:溶解度(再結晶)
3種の不明の物質を、
実験によって識別していくよくある問題です。
ですが、会話文形式の問題となり、
会話文から必要な情報を引き出す必要があります。
その一部を以下に示します。
| [会話文] 令子:水への解けやすさの違いを利用して、物質A, B, C が何であるかを区別してみましょう。まずは10℃の水100gに、物質A, B, C をそれぞれ25gとかしてみましょう。 和夫:物質Aだけがすべてとけ、物質B, C はとけ残りがありました。物質Aが何であるかは、わかりそうです。 令子:次に、40℃の水100gに物質A, B, C をそれぞれ50gとかしてみましょう。 和夫:物質Bはすべてとけましたが、物質A, C にはとけのこりがありました。 |
(1)物質A, B, C は硝酸カリウム、塩化ナトリウム、ミョウバンのうちどれか。それぞれあてはまるものを書け。
上記の和夫くんの初めの文言から、
10℃で25gが全てとけているので、
Aは「塩化ナトリウム」であることが図1のグラフから読み取れます。
次に和夫くんの次の文言から、
40℃で50gが全てとけているので、
Bは「硝酸カリウム」であることがグラフから読み取れます。
よって、最後のCは残った物質となるので、
答えは「A:塩化ナトリウム、B:硝酸カリウム、C:ミョウバン」ですね。
理科も読解の時代です。
しかも、文章だけではなく
文章からグラフという2つのものを
「言い換えた」表現の理解が重要となります。
文章や図に示されていることから、
「つまりどういうことなのか?」
を考えなければ、問題は解けないのです。
丸暗記時代は昭和平成で終了であることは
お分かりいただけるでしょうか?
(2)50gの物質Bを40℃の水100gにとかしたとき、さらに何gの物質Bをとかすことができるか。会話文中の( X )に当てはまるものとして適切なものを次のア〜エから選べ。
和夫:物質Bは40℃の水100gにさ、さらに( X )とかすことができます。
ア:約6g
イ:約14g
ウ:約22g
エ:約28g
そもそも、溶解度の定義を知らなければ
この問題は解くことができません。
溶解度は、
「100gの水に、限界までとける物質の質量」
のことを指します。
そして、溶解度は水の温度によって
物質ごとに変化します。
では図1の溶解度曲線の情報をまとめておきます。
硝酸カリウム 40℃:約63g
この問題を考えるときに、
「硝酸カリウムが63g入るコップに、50gを加えた。あと何g入るか?」
と問われていると考えるとよく理解できるでしょう。
小学生でも十分分かります。
大事なことは言葉の意味の理解、
理科で言えば定義の理解です。
答えは、「イ」ですね。
(3)100gの水に物質Aを25gすべてとかしたときの質量パーセント濃度は何%か。
「%」。
これが出た時点で思考停止する生徒もいます。
意味が理解できていないからですね。
以下の図で考えてみましょう。
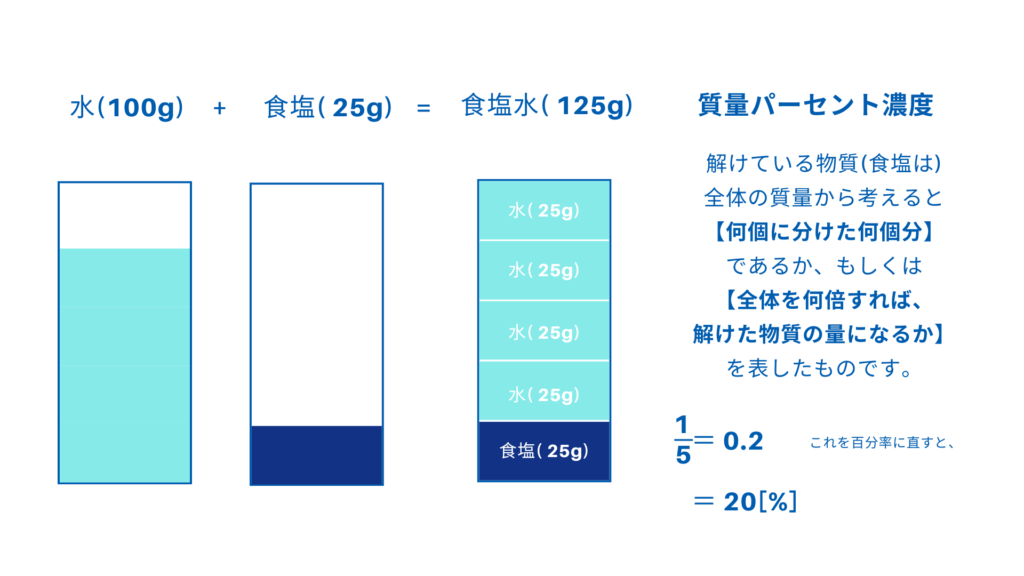
さぁ、何か難しいところはあったでしょうか?
このように、言葉を図に直して「言い換える」ことで
単に言葉で理解するよりも、スッと頭に整理されるから
面白いですよね。
問題を解くときに、常にじゅくちょーが
「図に直して考えてきなさい。」
と言っている意味はここになります!
(4)100gの水に物質Bを50gすべてとかした水溶液にさらに水を加え、(3)の質量パーセント濃度と同じ濃度にするためには、水を何g加えるとよいか。
(3)ができていなければ解けない問題です。
いやらしいですね。
問われていることはつまり、
質量パーセント濃度20%の硝酸カリウム水溶液を作るために、
水があと何g必要かということです。
先ほどと同様に、図で考えてみることにしましょう。
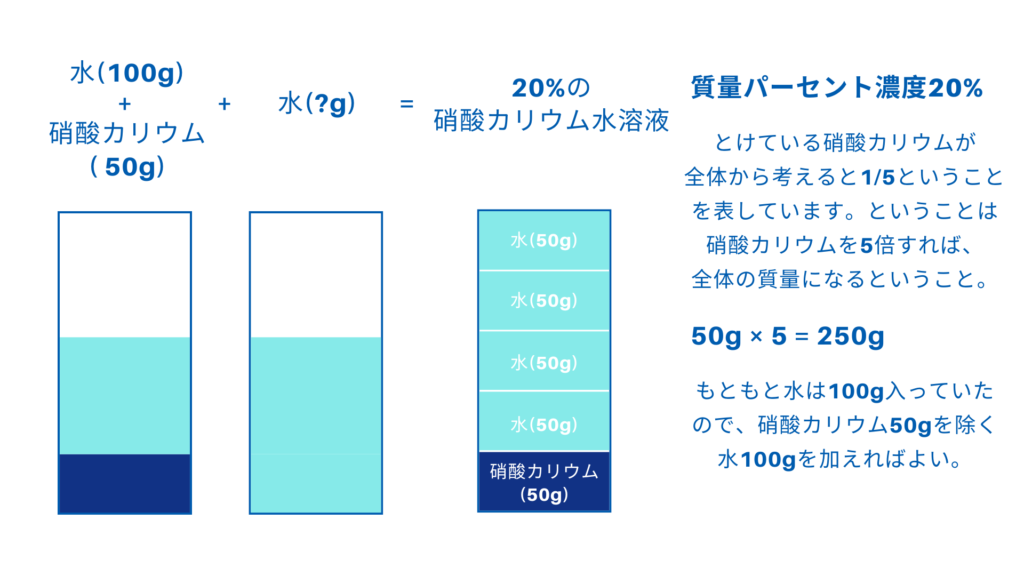
さぁ、いかがでしょうか?
この図で考えれば、
何の難しさも感じないのではないでしょうか。
(5)物質をいったん水にとかし、温度を下げるなどして、再び決勝として取り出す作業を何というか。
これは簡単ですね。
答えはもちろん、「再結晶」です。
(6)下線部(水溶液の温度を下げても結晶をほとんど取り出すことができない物質もあります)について、次の①、②の問いに答えなさい
① 水溶液の温度を下げても結晶をほとんど取り出すことができない物質は、硝酸カリウム、塩化ナトリウム、ミョウバンのうちどれか。
② ①の物質の水溶液の温度を下げても結晶をほとんど取り出すことができない理由を、「溶解度」という語を用いて、簡潔に説明せよ。
①の答えは、「塩化ナトリウム」ですね。
もちろんその理由としては、
「②水溶液の温度が変化しても、ほとんど溶解度の変化がないから」
となります。
これも理由を問う問題ですが、
ベタすぎることもあり
暗記してしまっている内容でしたね。
ということで、中1化学の問題の終了です。
難易度的には、計算問題系の部分で
意味理解ができていない生徒は
撃沈だったことでしょう。
上記の図の解説でわかる通り、
意味さえ理解していれば小学生でも
十分簡単に解ける問題なのです。
公式暗記は、意味が理解できている人が
便利に使いこなすツールです。
学習の仕方をアップデートさせて高校に
進学しなければ、高校の学習には
全くついていけなくなってしまいますよ!
大問8【中2化学】:酸化還元反応
この単元も、図で言い換えて考えると
非常に簡単な問題となります。
問題文に書かれた情報を整理すると
以下のようなものになります。
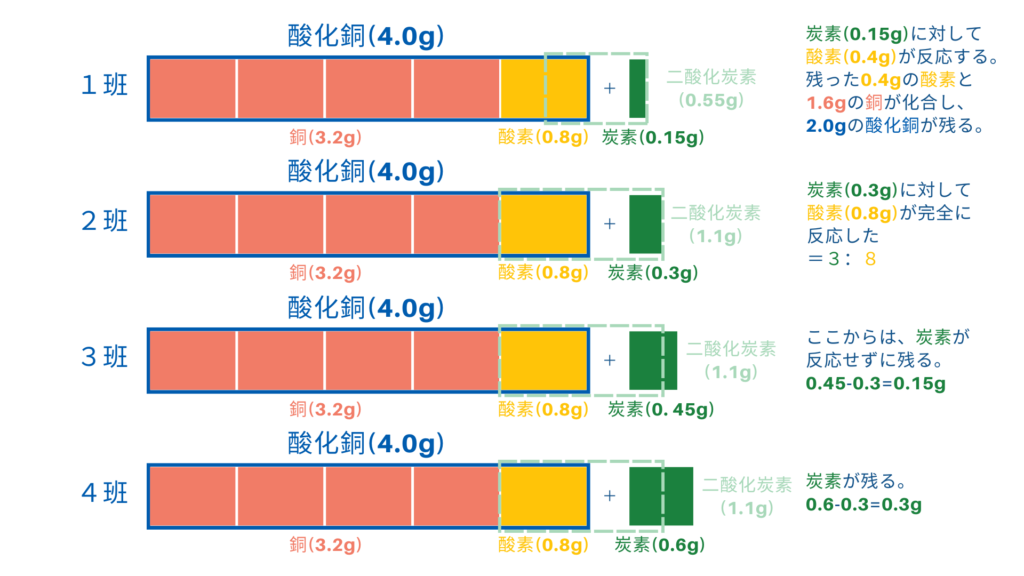
(1)酸化銅と活性炭(炭素)の混合物を加熱したときに起こる化学変化を、化学反応式で表せ。
書かれている言葉をそのまま化学式で書けば大丈夫ですね。
「CuO + C → Cu + CO2」
しかしこれでは、左辺と右辺の原子の数が合いません。
右辺に、Oが2つあるので、左辺のCuOの数を増やします。
「2CuO + C → Cu + CO2」
そうすると、右辺のCuの数が合わなくなるので、
「2CuO + C → 2Cu + CO2」
これで、綺麗に数が整いました。
(2)次の文は、酸化銅と活性炭(炭素)の混合物を加熱したときに起こる化学反応について説明したものである。( ① )〜( ⑤ )にあてはまる語を書け。ただし、物質については化学式ではなく、物質名で書くこと。
酸化銅は( ① )されて( ② )になり、活性炭(炭素)は( ③ )されて( ④ )になった。このことから、銅と炭素では( ⑤ )の方が、酸素と結びつきやすいことがわかる。
現象の理解を問う、用語問題ですね。
酸化銅は酸素を失います。
よって、「① 還元」です。
その結果、元の物質へと戻り
「② 銅」となりますね。
炭素の方は、酸化銅の酸素と結びつきますから
よって、「③ 酸化」となります。
その結果、炭素と酸素が結びつき
「④ 二酸化炭素」になりますね。
もちろん、これらの結果から
酸素が結びつきやすいのは
「⑤ 炭素」だと言えるでしょう。
(3)下線部a(目玉クリップでゴム管を閉じて)の操作をする理由を書け。
これ系の問題で、何も考えず脊髄反射的に
解答を書いてしまった誤答としては
「石灰水が逆流しないようにするため」
「逆流した液体が加熱部に触れ、試験管が破損することを避けるため」
などが挙げられるでしょう。
問題文に、
「機体の発生が終わった後、ガラス管を石灰水から引き抜き、火を消した。」
とあります。
この操作から、上記の理由はあり得ないことになります。
問われていることに正確に答えること。
「何について」を四角で囲み、
「どのように」の部分を波線で引く。
国語指導と同じことを全教科に広げていくことが
いかに大切であるかを物語る問題でした。
答えは、
「試験管Aの中へと酸素が入り込んでしまうことで、還元された銅が再び酸化してしまう可能性があるため。」
でオッケーです!
(4)1班、3班、4班について、試験管Aに残った黒色粉末はそれぞれ何か。もっとも適切なものを次のア〜ウからそれぞれ選べ。
ア:酸化銅
イ:炭素
ウ:酸化銅と炭素の混合物
もう一度、冒頭の図を示してみます。
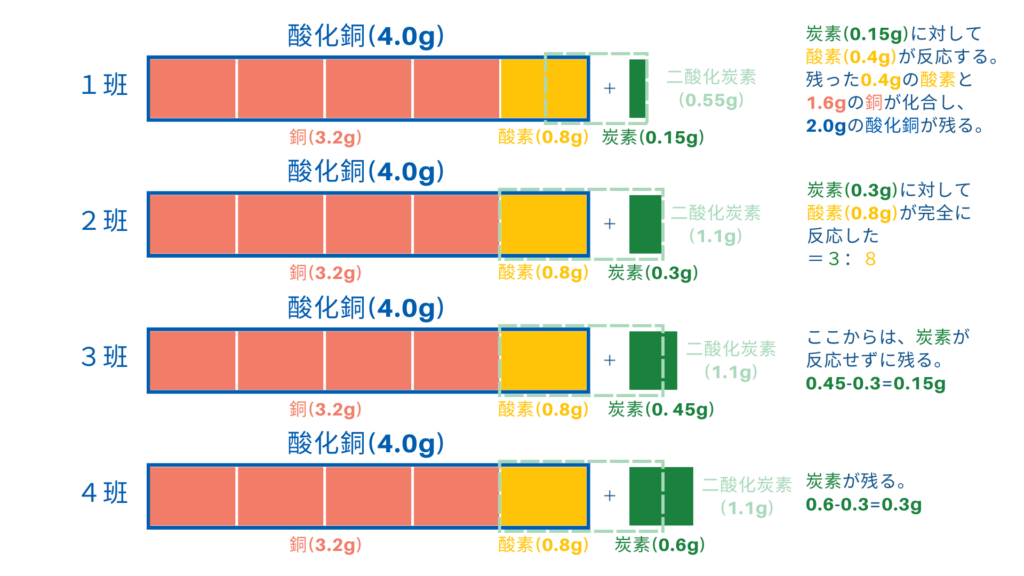
言葉と表で示された情報を
図で言い換えて翻訳することで、
この実験でどのような化学現象が
起こっているのかがみて取れます。
答えは、「1班:ア、3班:イ、4班:イ」ですね。
(5)表1のXにあてはまる数字を答えよ。なお、試験管Aの中では、酸化銅と活性炭との反応以外は起こらなかったものとする。
もう一度、冒頭の図を示してみましょう。
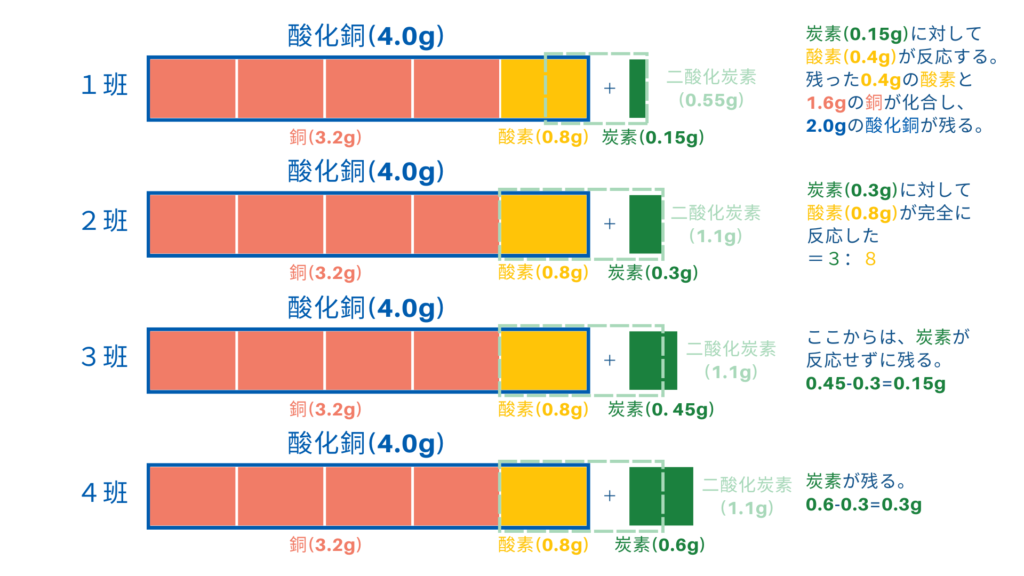
1班の図と解説をご覧ください。
0.15gの炭素では、酸化銅に結びついている酸素が
全て反応しないことが分かります。
反応した0.4g分だけ酸化銅4.0gから奪われますので、
答えは、「3.6g」となりますね。
化学講評:やや難!?
全分野の解説が終わりました。
伝えたいことは、昨日の結論と変わりません。
「これはどうなる」
という一問一答の知識だけではなく
「なぜそうなる」
の理由や根拠、原理原則などの知識が必要不可欠です。
とにかく、
「無意識で努力し続ける伸びる学習習慣を持つ生徒」
がいる受験という分野において
「そこそこの努力で伸びない学習習慣を持つ生徒」
が上位に食い込もうとするのは
並大抵のことではありません。
学習の成果は、「質」と「量」の両輪です。
どちらも伴うことで、力強く進むことができます。
基礎学は自分の学習の仕方を改めることを
教えてくれるいい機会となっています。
高校からの当たり前に自分を成長させていきましょうね!
ちゃん♪ちゃん♫
いろんな質問にもここでお答えするよ!下のLINEからご質問どーぞ!
校
じゅくちょーの共著としての書籍第二弾、
『11人の敏腕塾長がこっそり教える 地方名門国公立大学 合格バイブル〜親子で読むと勉強にすぐ結果が出る!〜』
が発刊されました!
徳島という地方の受験生たちが、情報弱者として受験に対して後手に回らないためのお役立ち本間違いなし!
ぜひ、お近くの書店やAmazonにてご購入し、お手にとってお読みいただければ幸いです!(2022.8.20時点:勉強法のカテゴリーで現在17位!)
そして、第一弾となるKADOKAWAから出版された、
『自学力の育て方』も絶賛発売中です!




